Hvers vegna er kolum brennt í kísilverum? Hvaða efnahvörf verða? Gengur kolefnið í þeim í samband við kísilinn? Er þá einhver losun á CO2?Kísilver eru hluti þess sem við nefnum orkufrekan iðnað á Íslandi. Tvö kísilver hafa verið reist á Íslandi á undanförnum árum gagngert til að framleiða kísilmálm, annað þeirra í Helguvík en hitt á Bakka við Húsavík. Hvorugt þeirra er í rekstri í dag hvað sem síðar kann að verða. Á Grundartanga í Hvalfirði hefur járnblendiverksmiðja Elkem verið starfrækt í fjóra áratugi en þar er framleiddur kísilmálmur með um 75% kísilinnihaldi sem blandaður er með 25% járni (FeSi) og er sérhæfður til íblöndunar í stáliðnaði og í járnsteypu. Í meginatriðum fer framleiðslan eins fram í öllum þessum verksmiðjum.
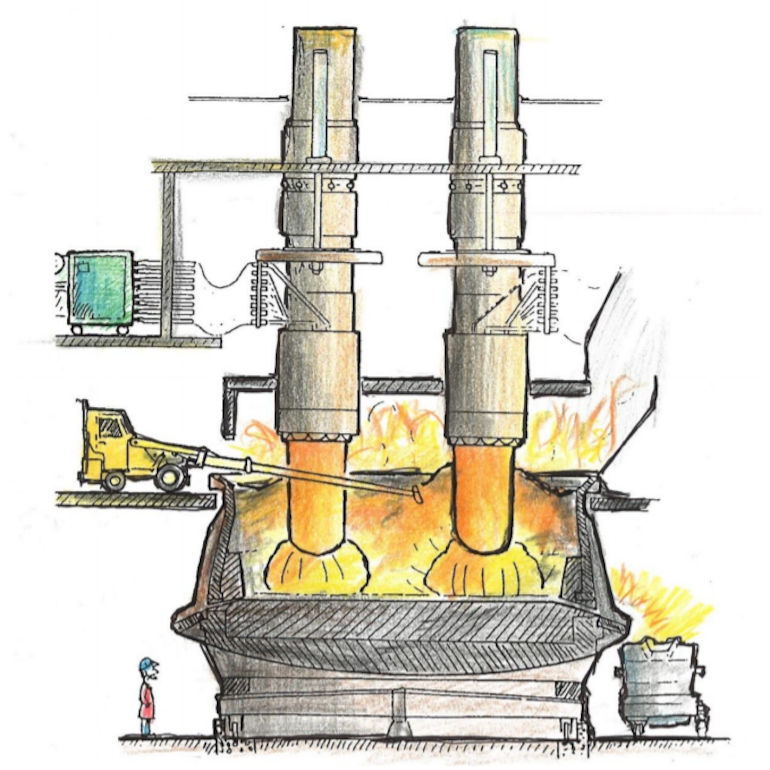
Mynd 1. Ljósbogaofn séður frá hlið. Til einföldunar sjást ekki nema tvö af þremur skautum. Uppi á milligólfi er tæki að störfum við að skara í ofnfyllunni. Neðst í ofninum safnast fyrir bráðinn málmur (hér 75% Si og 25% Fe), sem eftir þörfum er tappað af í ker hægra megin á gólfinu. Til vinstri á gólfinu er maður að fylgjast með. Hann gefur okkur tilfinningu fyrir stærðarhlutföllum.
SiO2 + 2C → Si + 2CO (i)Hér hefur kísillinn verið afoxaður niður í kísilmálm eins og efnafræðingar segja og kolefnið hefur oxast í kolmónoxíð (einnig nefnt koleinildi), sem er baneitruð gastegund. Til að forða því að verksmiðjan spúi út frá sér ógrynni af eitruðu gasi er lofti (og þar með súrefni) blandað saman við heitan útblásturinn frá ofninum og oxast þá kolmónoxíð yfir í koldíoxíð (einnig nefnt koltvíildi) í reykháfnum og reykhreinsibúnaði:
2CO + O2 → 2CO2 (ii)Með því að leggja saman jöfnur (i) og (ii) fáum við sem heildarhvarf:
SiO2 + 2C + O2 → Si + 2CO2 (iii)Lítum nú aftur á spurningarnar. Kol eru notuð í kísilverum til að bindast súrefninu í kvartsinu. Efnahvörfin sem sett hafa verið fram gefa mjög einfalda mynd af ferlinu í ofninum og jú, vissulega er losun á koldíoxíði veruleg.
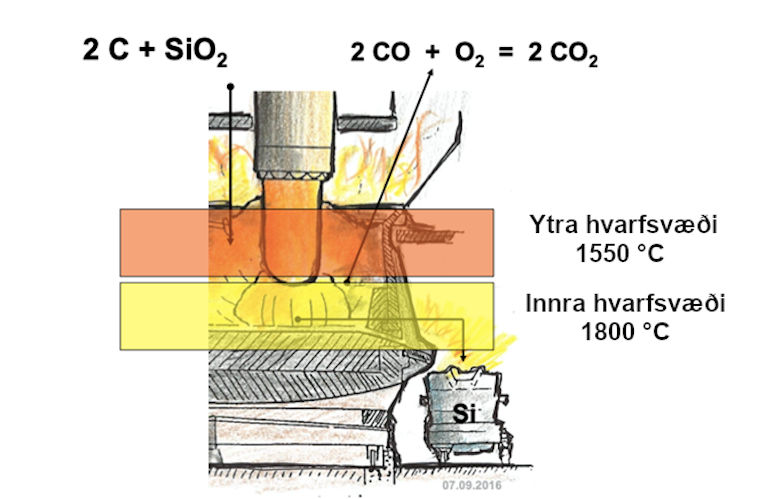
Mynd 2. Þessi mynd sýnir tvennt. Annars vegar að ofan til vinstri hvaða efni fara inn í ofninn og svo til hægri hvaða efni fara út úr ofninum. Til viðbótar sýnir myndin líka tvö misheit hvarfsvæði innan ofnsins. Efra og ytra svæðið er um 1550 °C heitt og svo innra svæðið neðar í ofninum umhverfis ljósbogann þar sem hitastigið fer yfir 1800 °C.
- Rafskautin eru notuð til að ná upp miklum hita neðst í ofninum. Það gerist þannig að ljósbogi myndast milli skautanna og bráðins málms á botni ofnsins. Þess vegna er ofn af þessari gerð kallaður ljósbogaofn. Án ljósbogans næst ekki nægilega hátt hitastig til að hvarf (i) eigi sér stað.
- Efnahvörfin í ofninum eru talsvert flóknari en jöfnur (i) til (iii) gefa til kynna. Þannig má skipta ofninum í tvö misheit hvarfsvæði og samspil mismunandi hvarfa eiga sér stað á milli þeirra.
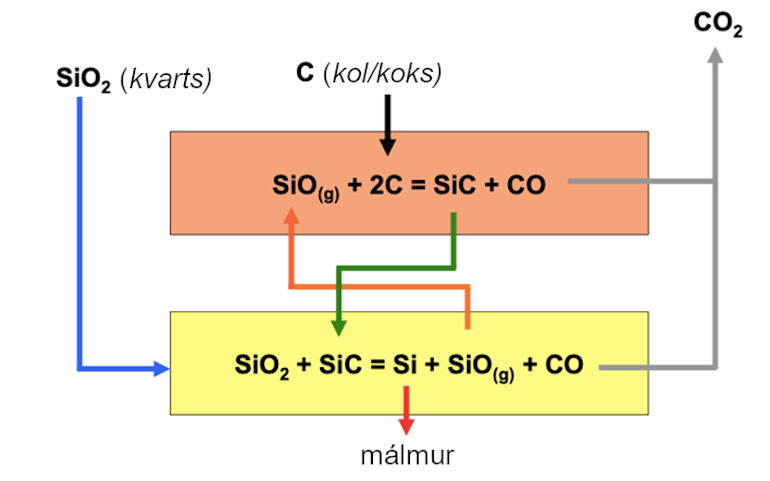
Mynd 3. Hér er búið að setja inn á hvarfsvæðin tvö á mynd 2 þau efnahvörf sem þar fara fram. Ef við skoðum neðra og heitara hvarfsvæðið fyrst, þá sígur óhvarfað kvarts (SiO2) þangað niður og hvarfast við kísilkarbíð (SiC), sem kemur úr efra hvarfsvæðinu og myndar bráðinn kísilmálm og kísilmónoxíð gas (SiO(g)) auk kolmónoxíðs. Kísilmónoxíð stígur upp í efra hvarfsvæðið og hvarfast þar við kol og myndar kísilkarbíð, sem sígur niður í neðra svæðið og kolmónoxíð, sem stígur upp úr ofninum og endar sem koldíoxíð samkvæmt jöfnu (ii).
- ^ Nú vill svo til að fyrir sléttu ári fóru fram greinaskrif á vefritinu „Kjarninn“ um framleiðsluferlið á Bakka eða nánar til tekið „kolabrennsluna á Bakka“ og er hentugt að vísa til þeirra varðandi nánari lýsingar sjá heimildir [1] til [3].
- [1] Ingvar Helgi Árnason. (2019, 11. september). Kolabrennslan á Bakka. Kjarninn. (Sótt 21.9.2020).
- [2] Kári Stefánsson. (2019, 12. september). Þegar tilgangurinn á að helga meðalið. Kjarninn. (Sótt 21.9.2020).
- [3] Ingvar Helgi Árnason. (2019, 14. september). Svar til Kára. Kjarninn. (Sótt 21.9.2020).
- Myndir: Þorsteinn Hannesson. (2016). The Si process. Elkem Iceland. (Sótt 21.9.2020). .
