Hver er algengasti afritunarfjöldinn (e. cycle threshold) í kjarnsýrugreiningum á Íslandi vegna veirunnar SARS-CoV-2?Til að svara þessari spurningu þarf fyrst að útskýra hugtakið kjarnsýrumögnun (e. polymerase chain reaction, PCR) og setja það í samhengi við COVID-19 (sem orsakast af veirunni SARS-CoV-2). Kjarnsýrumögnun magnar upp sértæka búta af erfðaefni með notkun vísa (e. primer), sem bindast aðeins við vissar raðir erfðaefnis. Erfðaefnið er magnað upp með endurteknum „hringjum“ (e. cycle) af efnahvörfum. Sjúkdómsgreining á COVID-19 fer þannig fram að PCR er notað til að greina hvort sértækar erfðaraðir úr SARS-CoV-2 séu til staðar í háls- og nefkoksstroki. Upprunalega gaf PCR annað hvort jákvætt eða neikvætt svar en með nýrri tækni er hægt að áætla magn erfðaefnis með því sem kallast rauntíma PCR. Rauntíma PCR hefur valdið straumhvörfum í veirufræði og er notað við greiningu fjölda veirusýkinga, meðal annars öndunarfærasýkinga, miðtaugakerfissýkinga, HIV (e. human immunodeficiency virus), lifrarbólgu B og C. Í öllum tilfellum er metið hvaða niðurstaða úr rauntíma PCR samræmist virkri sýkingu. Lesa má nánar um þetta efni í svari við spurningunni Hvernig eru veirur greindar í mönnum?[1] og einnig í svari við spurningunni Hvernig er vitað hvort COVID-19 smit sé óvirkt? Hvað þýðir það að sýni sé jákvætt en smit óvirkt?[2]
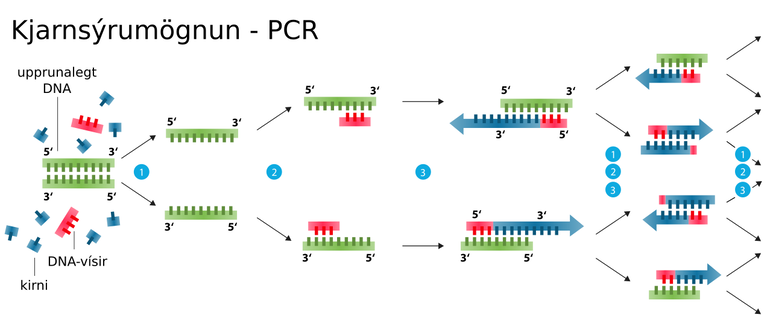
Skýringarmynd af kjarnsýrumögnun (PCR). Kjarnsýrumögnun magnar upp sértæka búta af erfðaefni með notkun vísa, sem bindast aðeins við vissar raðir erfðaefnis. Erfðaefnið er magnað upp með endurteknum „hringjum“ af efnahvörfum.
- Erna Magnúsdóttir. (2020, 19. mars). Hvernig eru veirur greindar í mönnum? Vísindavefurinn. (Sótt 14.12.2020).
- Erna Magnúsdóttir. (2020, 22. júlí). Hvernig er vitað hvort COVID-19 smit sé óvirkt? Hvað þýðir það að sýni sé jákvætt en smit óvirkt? Vísindavefurinn. (Sótt 14.12.2020).
- Cervik, M. o.fl. (2020, 19. nóvember). SARS-CoV-2, SARS-CoV, and MERS-CoV viral load dynamics, duration of viral shedding, and infectiousness: a systematic review and meta-analysis. The Lancet Microbe. (Sótt 14.12.2020).
- Zhu, N. o.fl. (2020). A Novel Coronavirus from Patients with Pneumonia in China, 2019. The New England journal of medicine, 382(8), 727–733. (Sótt 14.12.2020).
- Wu, F. o.fl. (2020). A new coronavirus associated with human respiratory disease in China. Nature, 579(7798), 265–269. (Sótt 14.12.2020).
- Zhou, P. o.fl. (2020). A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature, 579(7798), 270–273. (Sótt 14.12.2020).
- L'Huillier, A. G. o.fl. (2020). Culture-Competent SARS-CoV-2 in Nasopharynx of Symptomatic Neonates, Children, and Adolescents. Emerging infectious diseases, 26(10), 2494–2497. (Sótt 14.12.2020).
- Wölfel, R. o.fl. (2020). Virological assessment of hospitalized patients with COVID-2019. Nature, 581(7809), 465–469. (Sótt 14.12.2020).
- COVID-19 Investigation Team (2020). Clinical and virologic characteristics of the first 12 patients with coronavirus disease 2019 (COVID-19) in the United States. Nature medicine, 26(6), 861–868. (Sótt 14.12.2020).
- Arons, M. M. o.fl. (2020).Presymptomatic SARS-CoV-2 Infections and Transmission in a Skilled Nursing Facility. The New England journal of medicine, 382(22), 2081–2090. (Sótt 14.12.2020).
- Bullard, J., o.fl. (2020). Predicting infectious SARS-CoV-2 from diagnostic samples. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America, ciaa638. (Sótt 14.12.2020).
- La Scola, B. o.fl. (2020). Viral RNA load as determined by cell culture as a management tool for discharge of SARS-CoV-2 patients from infectious disease wards. European journal of clinical microbiology & infectious diseases : official publication of the European Society of Clinical Microbiology, 39(6), 1059–1061. (Sótt 14.12.2020).
- Le, T. o.fl. (2020). Severe Acute Respiratory Syndrome Coronavirus 2 Shedding by Travelers, Vietnam, 2020. Emerging infectious diseases, 26(7), 1624–1626. (Sótt 14.12.2020).
- To, K. K. o.fl. (2020). Consistent Detection of 2019 Novel Coronavirus in Saliva. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America, 71(15), 841–843. (Sótt 14.12.2020).
- McIntosh, K. (2020, 11. desember). Coronavirus disease 2019 (COVID-19): Clinical features. UpToDate. (Sótt 14.12.2020).
- Addgene. Polymerase Chain Reaction (PCR). (Sótt 14.12.2020).
- Public Health Ontario. (2020). An Overview of Cycle Threshold Values and their Role in SARS-CoV-2 Real-Time PCR Test Interpretation. (Sótt 14.12.2020).
- He, X. o.fl. (2020). An Overview of CyclTemporal dynamics in viral shedding and transmissibility of COVID-19e Threshold Values and their Role in SARS-CoV-2 Real-Time PCR Test Interpretation. Nature Medicine, 26, 672–675. (Sótt 14.12.2020).
- Kim, S. E o.fl. (2020). Viral kinetics of SARS-CoV-2 in asymptomatic carriers and presymptomatic patients. International Journal of Infectious Diseases, 95, 441-443. (Sótt 14.12.2020).
- File:Polymerase chain reaction.svg - Wikimedia Commons. (Sótt 14.12.2020). Upprunalegu myndina gerði Enzoklop og hún er birt undir leyfinu Creative Commons — Attribution-ShareAlike 3.0 Unported — CC BY-SA 3.0.

